AMG410 pan-KRAS 抑制剂|ChemAIRS AI 药物合成路线设计
2026 年 4 月,Daraxonrasib(RMC-6236),一款口服靶向药物,在晚期转移性胰腺癌的关键 III 期临床中,将患者的总生存期从传统化疗的 6.7 个月直接拉长至13.2 个月,患者死亡风险降低 60%。
这款改写癌王治疗历史的药物,瞄准的正是那个曾被医学界宣判“不可成药”长达 40 年的靶点,KRAS。
KRAS 是什么?
KRAS 基因,是调控细胞增殖与存活的核心“开关”。正常情况下,它收到生长信号就“打开”,推动细胞正常增殖;任务完成就“关闭”,让细胞进入正常凋亡周期。可一旦 KRAS 发生突变,这个开关就会被彻底焊死在开启状态,细胞会不受控制地疯狂增殖、侵袭转移,最终形成肿瘤。
更可怕的是,它几乎遍布所有高发恶性肿瘤,90% 的胰腺导管腺癌、30-44% 的结直肠癌、30% 的非小细胞肺癌,都能检测到 KRAS 突变。
但就是这个占比极高、危害极大的靶点,却由于其结构光滑,表面几乎没有能让药物分子牢牢结合的稳定口袋,在长达40年的时间里,让全球药企和科研人员束手无策。
直到全球首款 KRAS G12C 抑制剂获批上市,才终于撕开了这个不可成药靶点的第一道缺口。
AMG 410
2025 年 AACR 会议上,安进的 AMG 410 作为一款 pan-KRAS 抑制剂,首次公开亮相便惊艳全场,同年便在 clinical trials 网站登记启动国际多中心 Ⅰ 期临床研究(NCT07094113),计划入组 434 例多种 KRAS 突变实体瘤患者,快速推进临床转化。
作为新一代非共价、双功能 KRAS 抑制剂,AMG 410 通过结构优化,实现了对 KRAS 非活性(GDP 结合)与活性(GTP 结合)双构象的同时结合,解决了传统抑制剂仅能靶向失活态 KRAS、无法持续阻断致癌信号的核心痛点,更通过创新的大环化策略,攻克了同类药物透膜性差、口服受限的行业难题。
更值得关注的是,AMG 410 虽靶向与 KRAS G12C 抑制剂相同的变构位点,却实现了广谱的突变覆盖 —— 对 G12D、G12V、G12C、G13D 在内的多种 KRAS 高频突变体均展现出强效抑制活性,同时对 KRAS 具备高度选择性,相较于 HRAS、NRAS 靶点显示出极强的特异性,在非 KRAS 驱动的细胞中未观察到明显毒性。在 KRAS 突变型结直肠癌、胰腺癌、非小细胞肺癌的临床前模型中,AMG 410 已实现了显著的肿瘤缩小,有望惠及远超现有疗法的实体瘤患者群体。
这样一款突破性的分子,从实验室设计走向临床,第一道必须跨越的鸿沟,就是复杂结构的全合成。
ChemAIRS 为 AMG 410 打造两条差异化路线
对于 AMG 410 这类创新药分子而言,其分子结构中的多杂环体系、手性中心,尤其是核心的大环化结构,给逆合成路线设计带来了巨大挑战。
传统的逆合成设计,高度依赖资深合成化学家的个人经验,面对这类复杂分子,往往需要数月的时间反复试错、优化路线,不仅研发周期长、人力成本高,还可能面临路线可放大性差、副产物多、专利壁垒难以规避等问题,甚至可能因为合成难度过高,让极具潜力的候选分子止步于临床前研究。
在全球 KRAS 赛道内卷白热化的当下,合成效率早已不是研发的辅助环节,而是决定药企能否抢占临床先机、拿下赛道话语权的核心竞争力。
ChemAIRS,可为这类高难度复杂分子合成,提供全新的解题思路。
路线一:模块化拼接,兼顾反应稳定性与合成效率
该路线以易得的嘧啶并吡啶化合物为起始原料,先通过 4-位甲醚化、2-位引入吡咯并环片段,再引入硼酸酯完成核心中间体 9b 的构建;与此同时,以吡唑化合物 4a 为原料,经 Boc 保护、LDA 碱体系下的选择性烷基化、脱 TBS 保护,高效制备醇中间体 8b,完成另一关键片段的合成。
两大核心片段分别制备完成后,先将 7a 制备为活性碳酸酯与 8b 完成对接,再与中间体 9b 通过经典的 Suzuki 偶联反应实现片段拼接,最终经 Boc 与甲醚脱保护、基团活化、分子内 C-N 键环化,精准完成大环结构构建,顺利获得目标产物。
整条路线遵循 “片段模块化合成 - 精准偶联拼接 - 环化收尾” 的清晰逻辑,选用的均是工业化成熟的反应类型,官能团兼容性优异,原料廉价易得,反应条件温和可控,副反应少,不仅能高效完成目标分子的全合成,还可通过模块替换快速制备衍生物,为后续的结构优化与活性筛选提供了极大便利。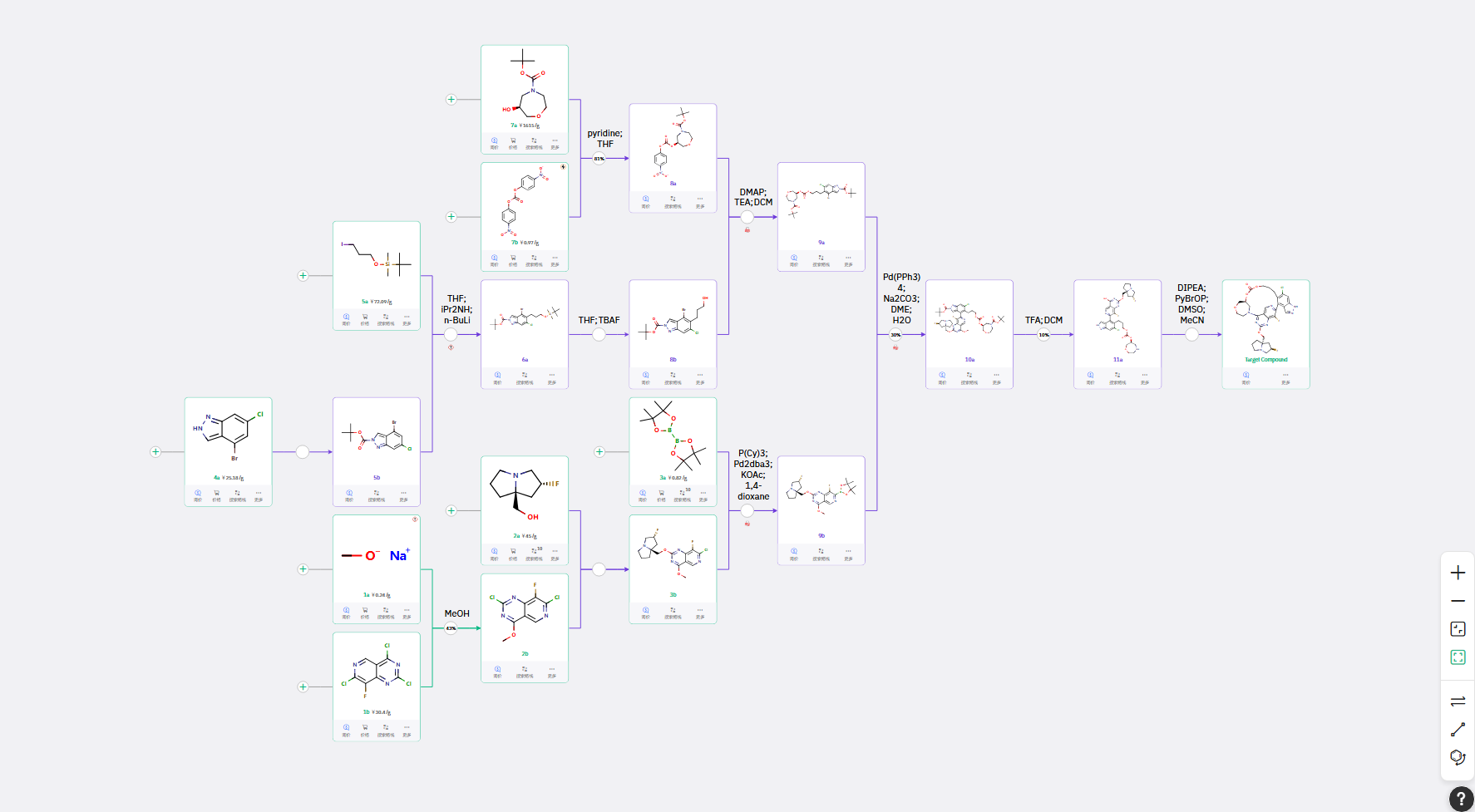
路线二:差异化策略,规避专利壁垒,优化工业化潜力
为了给药物研发提供更多选择,ChemAIRS 同时设计了第二条完全差异化的合成路线,从起始原料到偶联策略均实现了全新突破。
该路线以吡啶并嘧啶化合物为起始原料,先在 4-位引入三氟乙醇醚基团,再在 2-位接入含氟吡咯并环片段,与高吗啡啉衍生物 3a 反应后,进一步合成锡基化合物 7b,完成核心片段的制备;互补片段则以吡喃保护的吡唑化合物 5b 为原料,经烷基偶联、脱 TBS 保护制得,再与 7b 通过 Stille 偶联完成两大片段的高效拼接,后续经分子内碳酸酯合成完成大环构建,最终脱除吡喃保护基,获得目标产物。
这条路线通过保护基的差异化选择、偶联反应的策略调整,完美规避了现有路线的专利壁垒,同时进一步优化了反应的区域选择性,减少了手性中心的消旋风险,步骤更简洁,为后续的工业化放大生产提供了高可行性的备选方案。
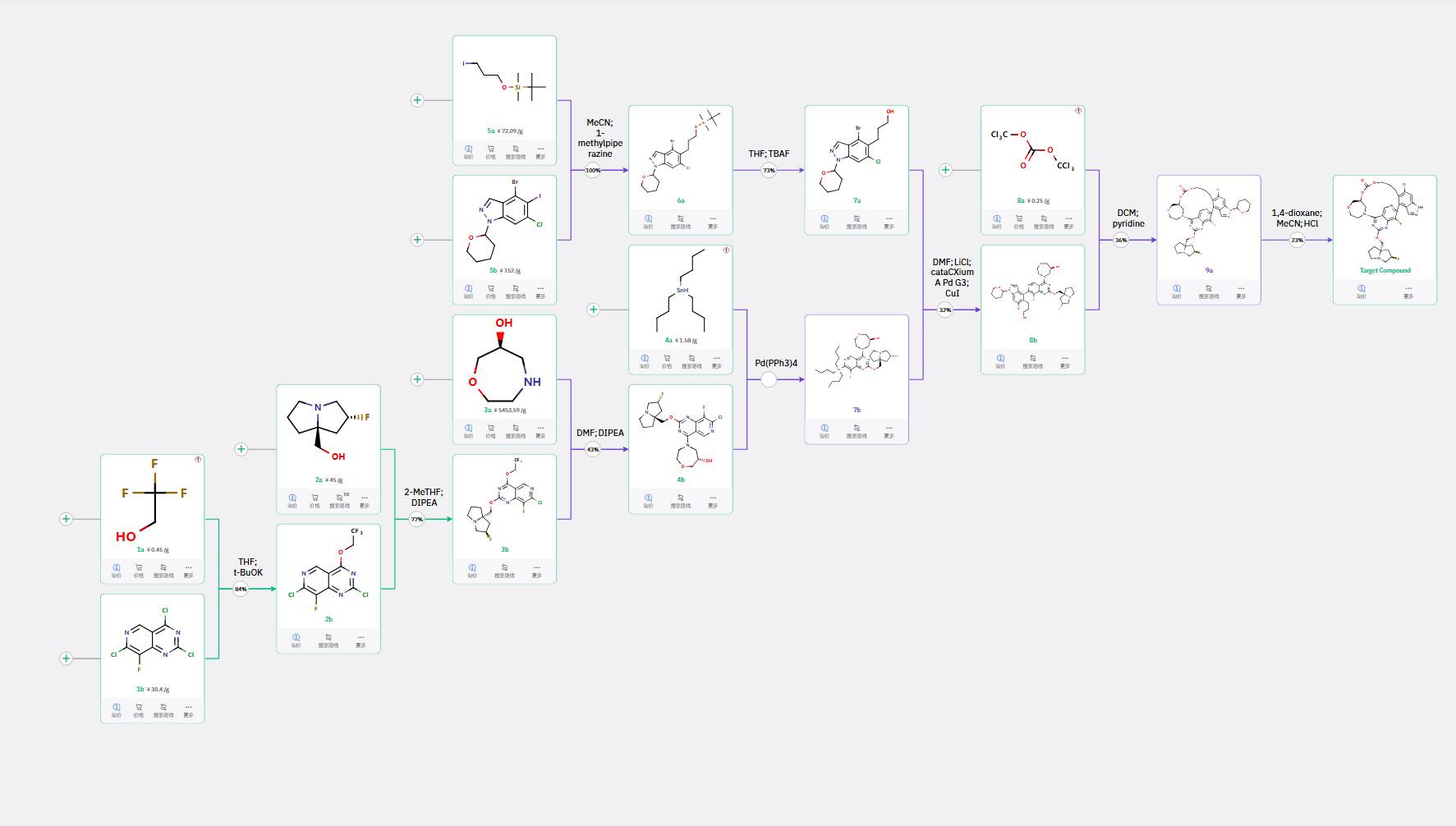
ChemAIRS,不止于路线生成
两条针对 AMG 410 的逆合成路线,只是 ChemAIRS 核心能力的一次展现。
ChemAIRS 的逆合成路线设计模块严格遵循反应步骤的先后逻辑、官能团的兼容性、手性中心的可控性等核心合成原则,尤其在 AMG 410 这类大环氨基酸、大环多肽化合物的合成中,精准实现了对手性氨基酸构建策略的合理利用,充分展现了其在复杂环系分子合成上的强大设计能力。
更具实用价值的是,研发人员可根据项目实际需求,设置或调整特定中间体为起始原料,自主缩短合成步骤,灵活规划项目节奏,最大程度压缩合成研发周期,降低研发成本。
无论是 AMG 410 这类 First-in-class 创新分子的全合成,还是同类分子的衍生物制备、专利规避路线设计,ChemAIRS 都能提供全新的合成方案与策略,真正实现了以数据和化学规则,驱动新药合成研发的效率革命。
如今,全球 KRAS 赛道从单一突变覆盖到广谱抑制,从共价结合到非共价双构象靶向,从单药治疗到联合用药。
AMG 410 的出现,为 KRAS 突变实体瘤患者带来了全新的治疗希望,而以 ChemAIRS 为代表的 AI 化学合成技术,凭借其在复杂分子逆合成设计上的硬核实力,正在成为新药研发领域不可或缺的核心基础设施,为全球生物医药创新,持续注入技术动能。