世界帕金森日:关注“颤抖中的生命”
当双手开始不自觉地颤抖,当稳健的步伐逐渐变得蹒跚,当曾经清晰的表达染上迟疑——帕金森病,这个被称为“不死的癌症”的慢性神经退行性疾病,正悄然改变着全球超过 1000 万患者的人生轨迹。设立于 1997 年的世界帕金森日,不仅是对詹姆斯·帕金森医生的纪念,更是向全社会敲响的警钟:关注帕金森,守护人类对抗衰老与疾病的尊严。
近日,Celon Pharma 宣布其 PDE10A 抑制剂 CPL’36 治疗帕金森病左旋多巴诱发运动障碍的 II 期临床试验结果强劲且积极。
PDE10A 为一种磷酸二酯酶,是纹状体信号通路的重要调节体,当其受到抑制后能够改善纹状体的失常状态,成为精神分裂症治疗的一个新的潜在靶点。
WO2015/177688 报道的合成策略如下,该路线为汇聚式路线。通过 1a 和 1b 完成关环后再将甲基进行氧化得到醛,然后与 5a(杂环肼类化合物)进行关环得到目标分子,总收率偏低。尤其是中间体 5a 的合成和其本身的稳定性可能存在较大的安全风险。
ChemAIRS 给出了如下单线合成策略。通过关环制备得到关键中间体 3a,再经官能团转化将氨基转化为溴,进一步经偶联反应得到中间体 5b,与 5a 完成关环构建嘧啶并咪唑环,再甲基化反应得到目标产物。单步反应均有较好的选择性,构建方案较为稳健可行,避开了较为危险的反应和中间体。
国家神经疾病医学中心、脑功能与脑疾病全国重点实验室、复旦大学附属华山医院郁金泰团队通过全基因组关联分析(GWAS)发现,神经元膜蛋白 FAM171A2 是病理性 α-synuclein 的关键受体,其通过选择性结合并内吞 α-synuclein 纤维,诱导神经元内单体错误折叠,进而导致神经元死亡和病理扩散。FAM171A2 提供了新的治疗靶点,有望从疾病早期对帕金森病进行干预,延缓疾病进展。复旦大学团队进一步通过 AI 筛选发现的小分子,可阻断 α-synuclein 与 FAM171A2 结合,动物模型中神经元损失减少 68%,目前已申请国际专利。
CN115504967 给出如下单线合成方案。将起始原料完成酮的保护后进行硝基的还原,然后引入官能团与肼类化合物进行关环,再脱保护与四氢吡略做还原胺化,进行拆分得到目标分子。
ChemAIRS 给出了如下合成策略。通过还原胺化拆分再进行硝基还原得到中间体 6a,1a 经 C-N 偶联反应得到 2b,进一步与苄胺衍生物反应再脱去引入氨基,最后与 6a 反应得到目标产物。整体路线汇聚式,将关键中间体进行合成后再对接,将拆分步骤前置提高路线的效率。
富含亮氨酸重复序列激酶 2(LRRK2)的活性升高与帕金森病的发病机制相关。由于存在穿越血脑屏障(BBB)这一艰巨挑战,寻找有效的 LRRK2 抑制剂的工作受到了阻碍。韩国世宗大学 Hwangseo Park 团队与韩国科学技术院 Sungwoo Hong 团队[1] 通过对生化功效和血脑屏障通透性进行精细的计算和合成优化,对体外和体内有效性进行评估,并结合药理学分析,发现如下化合物是一种很有前景的治疗帕金森病的新型先导化合物。
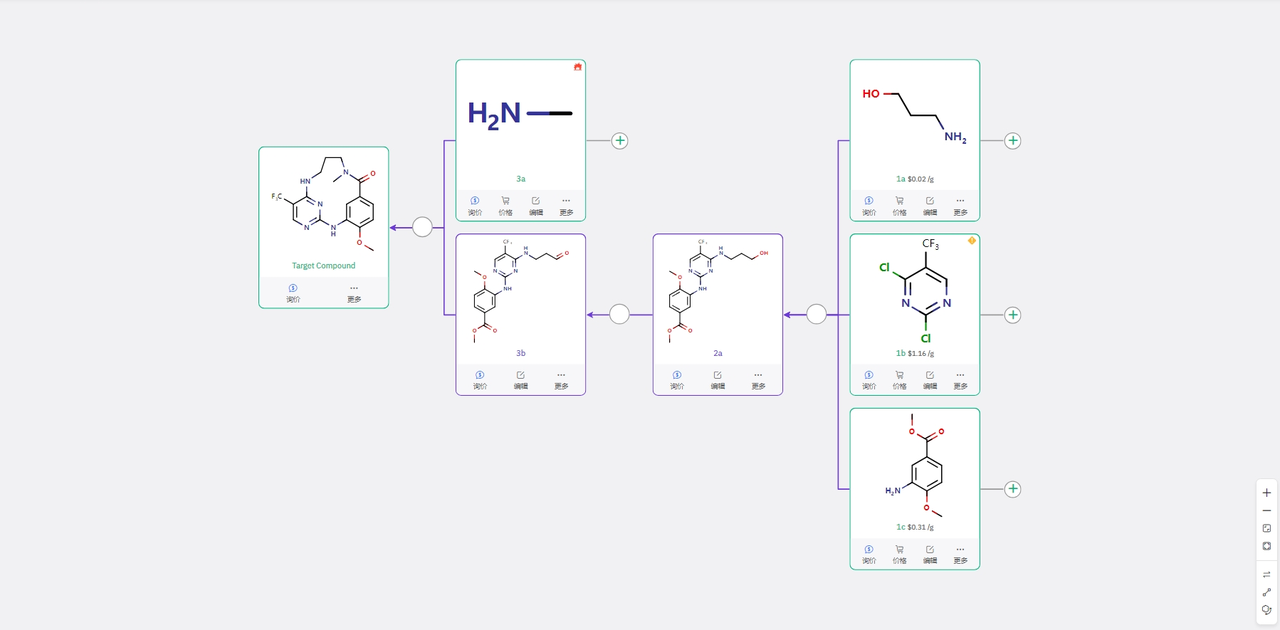
报道的单线合成方案如下。在起始原料 2,4-二氯嘧啶结构上先进行SNAr 取代反应,缩合后,再次进行取代反应完成关环,得到目标分子。
ChemAIRS 给出了如下汇聚式合成方案。在起始原料 2,4-二氯嘧啶结构上先后完成取代反应,羟基氧化成醛后再完成还原胺化和分子内的关环,得到目标分子。其中 2a 的合成可通过一锅法完成反应,目标产物的合成通过 3b 的还原胺化及分子内胺酯交换的一锅法完成关环。整体合成步骤为 3 步,效率较高。
参考文献: