9500万美元买一个“语法”?小分子合成的底层逻辑正在被重写
2026 年 2 月,纽约初创公司 Excelsior Sciences 宣布完成 9500 万美元融资,这笔巨额资金只为彻底重构小分子化学合成逻辑,让 AI 不仅能设计分子,更能直接指挥机器人将其制造出来。
这并非孤例。从清华大学靶向 RNA 的小分子 AI 预测平台 SMRTnet 登上 Nature Biotechnology,到南开大学苏波团队利用"乐高式"模块化策略将手性药物合成步骤缩短一半,再到国家自然科学基金委专门设立“自然-人工融合体系赋能复杂药物分子合成”重大研究计划——2026 年,小分子合成领域正迎来从“经验驱动”向“智能驱动”的跃迁。
01. AI 设计得了分子,却造不出来
小分子药物占 FDA 批准药物的三分之二,是现代医学的基石。但一个尴尬的现实是:虽然 AI 在分子设计环节已取得突破,化学合成本身却成为最大的瓶颈,常常将项目拖延数年。
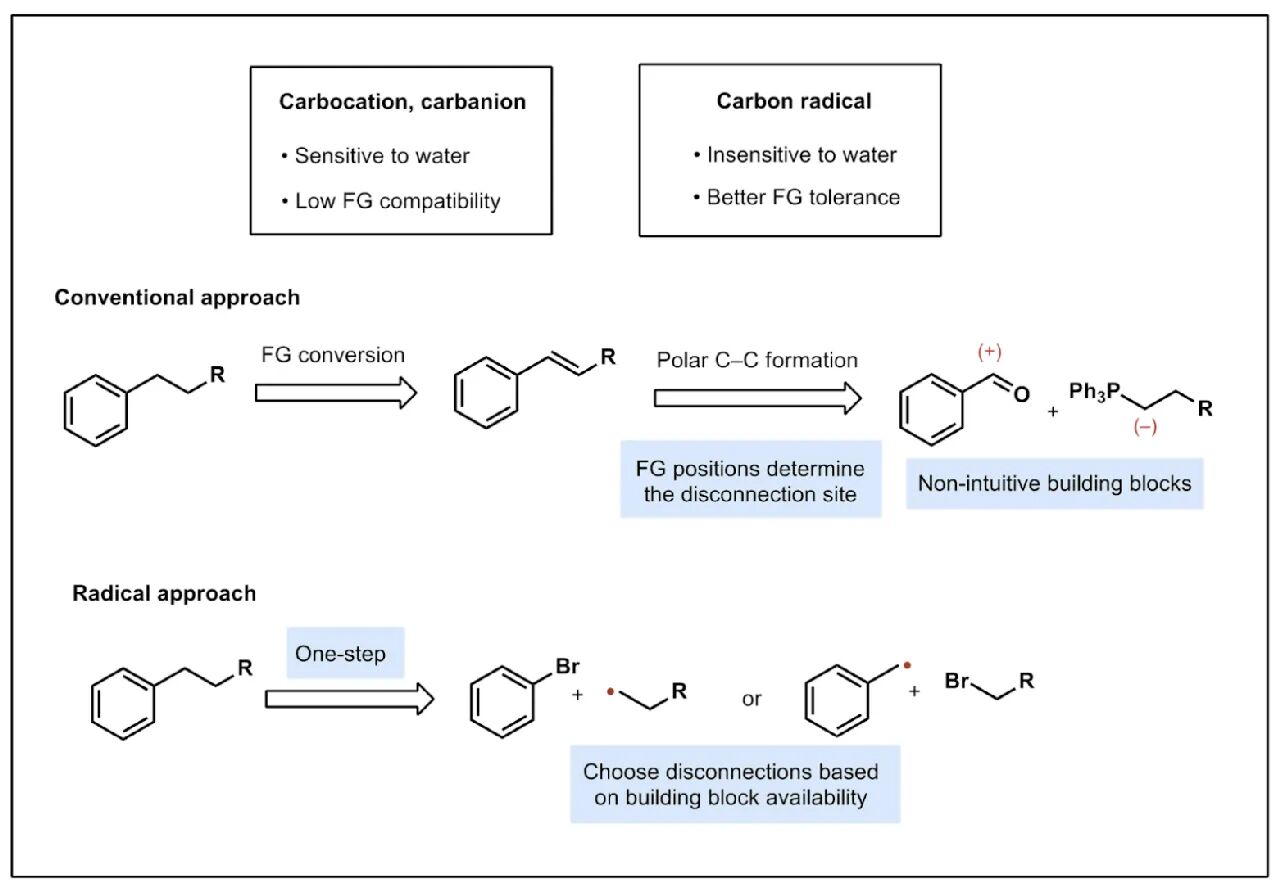
传统自动化化学系统试图“复制”人工操作——针对每种反应调试特定条件。这种方式效率低下,难以与 AI 设计的高通量需求匹配。正如 Excelsior CEO Michael Foley 所言:“我们需要一种能让 AI 系统和自动化平台在闭环中设计、制造、测试小分子的化学语言。”
02. “机器原生化学”是什么?
Excelsior 提出的解决方案极具启发性——“机器原生化学”(Machine-Native Chemistry)。其核心是开发“Smart Bloccs”技术平台:将合成单元转化为标准化、模块化的“砌块”,这些砌块成为 AI 可理解的“化学语言符号”,算法可直接指导分子构建。这种“迭代碳-碳键形成”策略,让 AI 从“纸上谈兵”的设计者转变为“指哪打哪”的指挥官。
03. 国内突破:从算法到工艺的闭环
2026 年 1 月,清华大学张强锋团队开发的 SMRTnet 方法登上 Nature Biotechnology。该方法仅需 RNA 二级结构信息,即可精准预测小分子-RNA 相互作用及结合位点,完全摆脱了对复杂三维结构的依赖。这为靶向 RNA 的小分子药物开辟了全新筛选路径。
在工艺层面,南开大学苏波教授团队实现了共轭二烯的催化不对称 1,3-硼胺化反应,建立了“乐高式”手性含氮杂环合成策略。以 2023 年 FDA 批准的药物伊普可泮为例,传统工艺需 8 步以上且必须手性拆分,而新策略将步骤缩短一半,直接避免拆分过程,显著降低成本。
04. 产业共振:CDMO 行业的智能化转型
小分子 API CDMO 正全面拥抱 AI。据 DCAT 报告,2026 年行业将呈现三大趋势:
1. AI 驱动的逆合成分析:整合实时供应链数据,动态调整合成路线,匹配工厂产能与库存。在这一领域,ChemAIRS 凭借其深度学习算法与强大的逆合成预测能力,已成为多家药企和 CDMO 的重要工具,助力研发团队在数分钟内完成复杂分子的路线设计与评估。
2. 预测性质量保障:通过实时监测和数据分析,在偏差发生前预警,加速批次放行。
3. 自动化与机器人:从生产到质检,半自主系统逐步普及,应对劳动力短缺并提升一致性。
Axplora 公司指出,到 2026 年,AI 和数字化将成为 CDMO 核心竞争力的分水岭——不仅能优化合成路线,更能预测设备适配性,最大化利用现有资产。
05. 化学合成的“ChatGPT时刻”?
当我们回顾 2026 年初的这些小分子合成突破,一个清晰的脉络浮现:化学正在从“手艺”变成“语言”。
从 Excelsior 的“智能砌块”到国家基金委的“自然-人工融合”重大计划,从 AI 预测 RNA-小分子相互作用到模块化手性合成——这些进展共同指向一个未来:AI 将理解化学合成的“语法”,并像生成文本一样生成分子。
2026年,小分子合成领域没有“颠覆”,只有“进化”。但正是这种从分子设计到工艺放大的全链条智能化,让化学这一古老学科焕发出新的生命力。